👁️ 網膜や視神経が悪くても白内障手術が必要な理由
── 「どうせ見えないから」で手術を諦めていませんか? ──
🌟 この記事のポイント
- 網膜や視神経に病気があっても、白内障手術で「見え方の質」は確実に改善します。視力表の数値だけでは測れない改善(まぶしさ軽減・コントラスト向上)が得られます[1–4]。
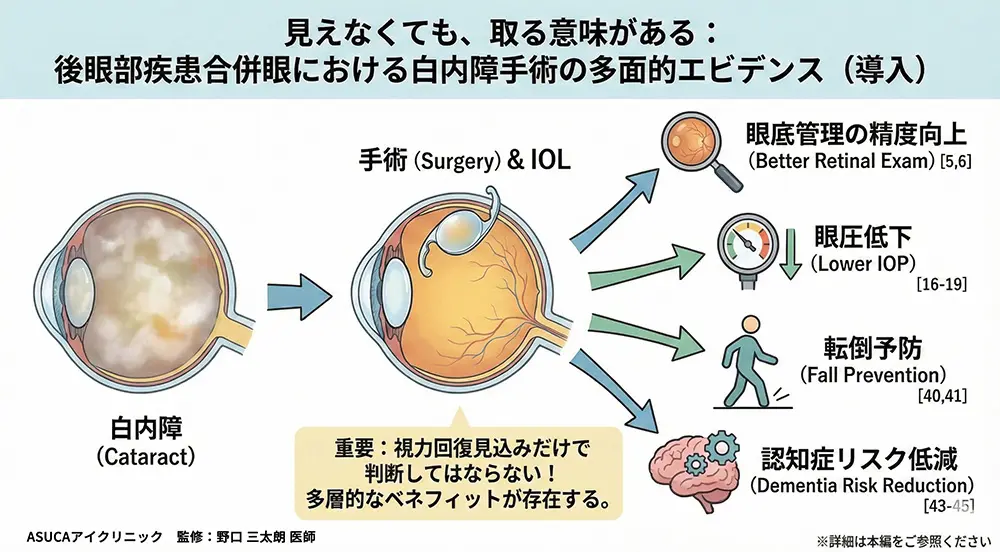
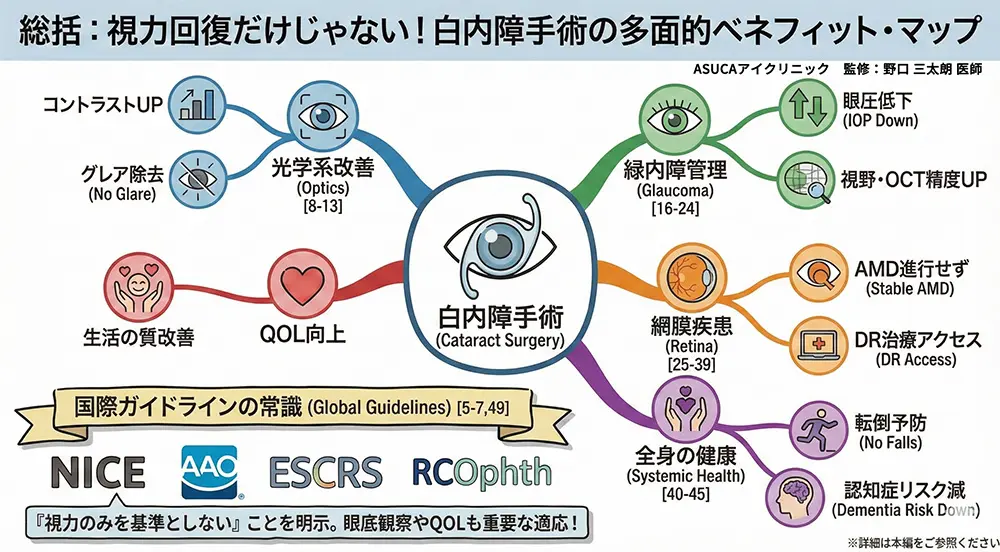
- 白内障手術には視力改善以外の大きなメリットがあります。眼圧低下(緑内障治療効果)[16,17]、転倒34%減少[40]、認知症リスク29%低下[43]、死亡率27〜46%低下[42,48]。
- 世界の主要ガイドライン(NICE, AAO, ESCRS)は「視力だけで手術の適応を判断してはならない」と明記しています[5–7]。
目次
- 【一般の方向け】🌟「網膜が悪いから手術しても意味がない」は本当?
- 🔍白内障手術で「見え方の質」が良くなる仕組み
- 😣まぶしさ(グレア)── 視力検査では見つからない悩み
- 💚緑内障があっても手術した方がいい3つの理由
- 🧡黄斑変性でも手術して大丈夫?
- 💛糖尿病網膜症と白内障手術
- 🏥転倒予防・認知症予防という驚きの効果
- 📋こんなケースではどうする?具体例で解説
- ❓よくある質問(FAQ)
- 📝【一般の方向け】まとめ
- 【眼科医向け】📐光学物理学的根拠
- 💧緑内障:IOP・視野・OCTの三重メリット
- 🔍AMD:AREDS2が示した安全性と視力改善
- 💉DR:治療アクセスと周術期リスク管理
- 🧠全身的アウトカム
- 📋国際ガイドラインの立場
- 📝【眼科医向け】まとめ
🌟【一般の方向け】1.「網膜が悪いから手術しても意味がない」は本当?
「緑内障で視神経が弱っているから手術しても見えるようにならない」「黄斑変性で黄斑がダメだから白内障は放置しましょう」──。このような説明を受けた経験はありませんか?
実はこの考え方は、最新の医学的知見とは大きく異なります。
世界中の研究が示しているのは、白内障手術の恩恵は「視力表の数字が良くなること」だけではないということです。白内障を取り除くことで得られるメリットは、実は非常に多岐にわたります[1–4]。
⚠️ 白内障を放置すると起きること
- 😣まぶしさ(グレア)がひどくなり、外出が億劫になる
- 🚶転倒のリスクが高まる(特にご高齢の方)
- 🧠認知症のリスクが高まる(最新の大規模研究で判明)
- 👁️緑内障や糖尿病網膜症の検査・治療の精度が落ちる
- 📈眼圧が高めに維持される(緑内障の方は特に不利)
🔍2.白内障手術で「見え方の質」が良くなる仕組み
🤔 視力だけではわからない「見えにくさ」
視力検査で「0.7が見えているから大丈夫」と言われたことはありませんか? しかし、実際の日常生活では「なんとなく見えにくい」「曇りガラス越しのようだ」という感覚が残っていることがあります。
これは、視力検査では測定できない「コントラスト感度」という視覚の質が低下しているためです[8,15]。
💡 わかりやすいたとえ
白内障のある目で世界を見ることは、汚れたフロントガラス越しに運転するようなものです。たとえ道路標識の文字(=視力)は読めても、全体が霞み、対向車のライトがまぶしく、雨の日は特に見えにくくなります。
白内障手術は、この汚れたフロントガラスを新品に交換することに相当します。たとえ目の奥の網膜に病気があったとしても、「フロントガラスを綺麗にする」効果は同じです[8,15]。
📊 具体的にどれくらい改善する?
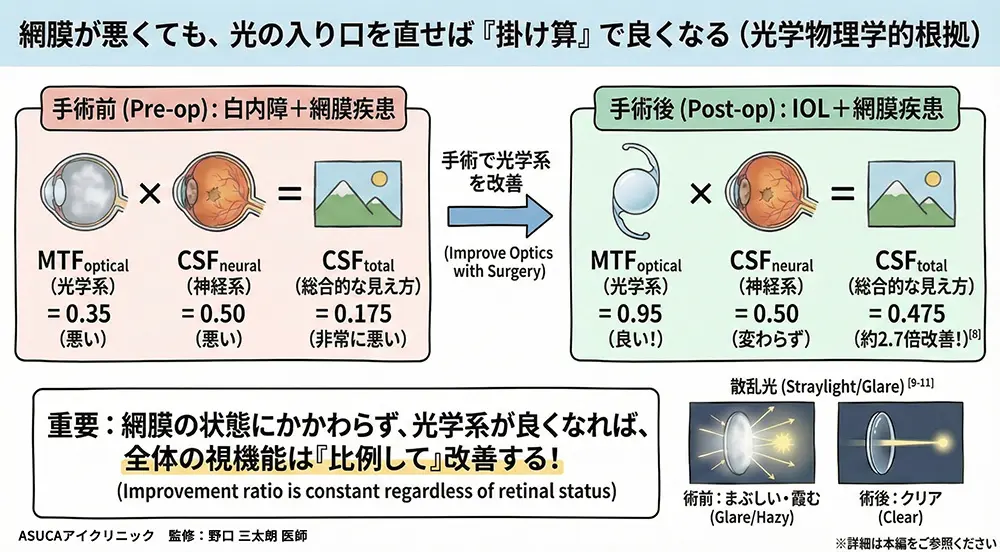
科学的には、見え方の質は「光学系の質 × 神経系の質」という掛け算で決まることがわかっています[8]。
見え方の質は「掛け算」で決まる
| 状態 | 光学系の質(白内障の影響) | 神経系の質(網膜の状態) | 見え方の質 |
|---|---|---|---|
| 白内障あり + 網膜正常 | 35%に低下 | 100%(正常) | 35%(悪い) |
| 白内障あり + 網膜50%障害 | 35%に低下 | 50%に低下 | 17.5%(とても悪い) |
| ✨ 手術後 + 網膜50%障害 | 95%に回復 | 50%に低下(変わらず) | 47.5%(大幅改善!) |
👆 注目してください!
網膜の状態が変わらなくても、白内障を取るだけで見え方は約2.7倍に改善します。これは数学的に証明されている事実です[8]。
😣3.まぶしさ(グレア)── 視力検査では見つからない大きな悩み
白内障がもたらすもう一つの深刻な問題が「まぶしさ」です。これは散乱光(ストレイライト)と呼ばれる現象が原因です[9–11]。
白内障の種類によって、まぶしさの程度は大きく異なります。
白内障のタイプ別「まぶしさ」の程度[11]
| 白内障のタイプ | まぶしさの程度 | 視力との関連 | 患者さんの訴え |
|---|---|---|---|
| 🟡 核白内障 | 中等度 | ある程度関連する | 「全体的にかすむ」 |
| 🟠 皮質白内障 | 中等度~強い | あまり関連しない | 「光がにじむ」 |
| 🔴 後嚢下白内障 | 非常に強い | ほとんど関連しない | 「視力は出ているのにとてもまぶしい」 |
⚡ 特に注目すべきポイント
後嚢下白内障(PSC)は視力が比較的良くてもまぶしさが非常に強いのが特徴です。視力検査だけでは白内障による障害を正しく評価できない典型例であり、緑内障合併眼ではさらに視野検査の信頼性まで低下させます[11,12]。
白内障手術後、まぶしさは1週間以内にほぼ正常レベルまで改善します[13]。
💚4.緑内障があっても手術した方がいい3つの理由
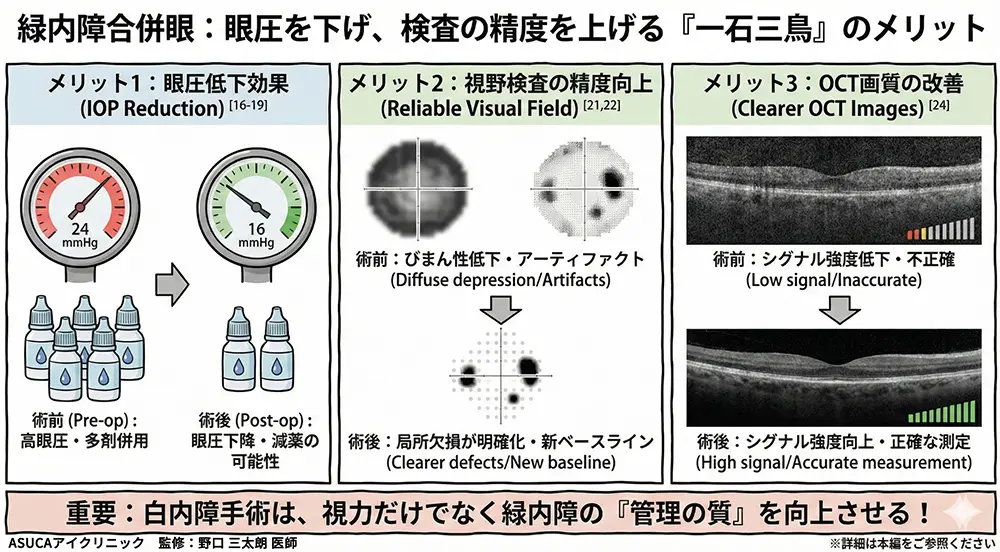
① 眼圧が下がる 📉
白内障手術をすると、多くの場合眼圧が下がります[16–19]。水晶体は加齢とともに厚くなっており、これを取り除いて薄い人工レンズに入れ替えることで、目の中の水(房水)の通り道が広がるためです。
- 開放隅角緑内障の方:平均で約2.7~8.5 mmHgの眼圧低下[16,17]
- 閉塞隅角緑内障の方:平均で約6.4~9.5 mmHgの眼圧低下[18]
- 点眼薬の減薬や、緑内障手術の回避につながる可能性
② 検査の精度が上がる 🔬
緑内障の管理で欠かせない視野検査やOCT(目の奥の断面写真を撮る検査)は、白内障があると精度が落ちます[20–24]。
- 白内障のせいで視野が実際より悪く見えたり、逆に本当の悪化が隠れてしまう
- OCTの画像がぼやけて、視神経の状態を正確に判定できない
- 白内障手術後、OCTの画質は平均24%向上する[24]
③ 目の奥がしっかり観察できるようになる 👁️
白内障があると、医師が目の奥(眼底)を詳しく観察することが困難になります。白内障手術により眼底観察が容易になり、緑内障の管理全体が正確になります。
🧡5.黄斑変性でも手術して大丈夫?
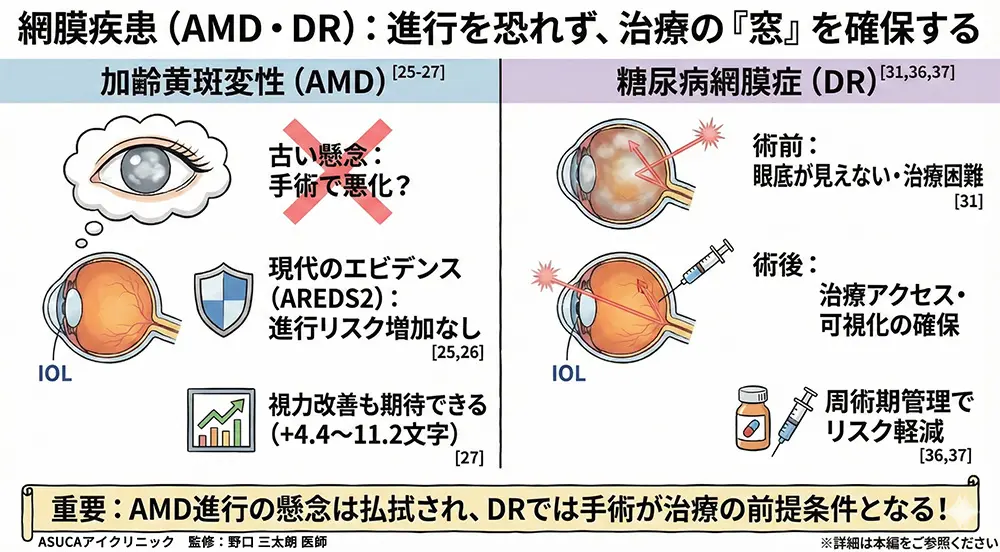
「白内障手術をすると黄斑変性が悪くなる」という心配をされる方がいますが、最新の大規模研究でこの心配は否定されています[25,26]。
📊 AREDS2研究(4,553眼、最長10年追跡)の結果[25]
白内障手術を受けた眼と受けなかった眼を比較した結果、黄斑変性の進行リスクに差はありませんでした。
米国国立眼研究所(NEI)は「AMD悪化への懸念から白内障手術を回避・遅延させる必要はない」と公式に声明を出しています[26]。
しかも、黄斑変性があっても白内障手術後に視力は有意に改善します[27]。
黄斑変性の重症度別・白内障手術後の視力改善[27]
| 黄斑変性の重症度 | 平均改善(ETDRS文字) | 有意性 |
|---|---|---|
| 🟢 軽度 | +11.2文字 | P < 0.0001 |
| 🟡 中等度 | +11.1文字 | P < 0.0001 |
| 🟠 高度 | +8.7文字 | P < 0.0001 |
| 🔴 血管新生型 | +7.5文字 | P < 0.0001 |
| 🔴 中心性地図状萎縮 | +4.4文字 | P = 0.005 |
✨ 最も進行した「中心性地図状萎縮」でも有意な改善が得られています。
重度両眼性AMDの患者さんでは、QOLスコアが44.0 → 56.9に改善したとの報告もあります[28]。
💛6.糖尿病網膜症と白内障手術
🔍 なぜ手術が必要?
進行した白内障があると、目の奥が見えなくなります。これは患者さんにとって「見えにくい」というだけでなく、医師にとっても網膜の状態が確認できない=適切な治療ができないことを意味します[31]。
- レーザー治療が正確にできない
- OCTで黄斑浮腫の評価ができない
- 糖尿病網膜症の進行度が判定できない
つまり、糖尿病網膜症のある方における白内障手術は「視力を上げるため」だけでなく「今後の治療を可能にするため」という重要な目的があるのです。
⚠️ 注意点:術後のケアが大切
糖尿病網膜症の方は、白内障手術後に網膜症がやや進行するリスクがあることが分かっています[34,35]。しかし、適切な管理を行うことで大幅にリスクを下げられます[36–39]。
- ✅術中・術前の抗VEGF注射で、進行リスクを約63%低減できる[36]
- ✅炎症止めの目薬(NSAIDs)を90日間使用で、黄斑浮腫リスクを16.7%→3.2%に低減[37]
👨⚕️ 当院での取り組み
当院では糖尿病網膜症をお持ちの方の白内障手術に際し、網膜の状態を十分に評価した上で、必要に応じて周術期の抗VEGF治療や消炎治療を併用し、安全な手術を心がけています。
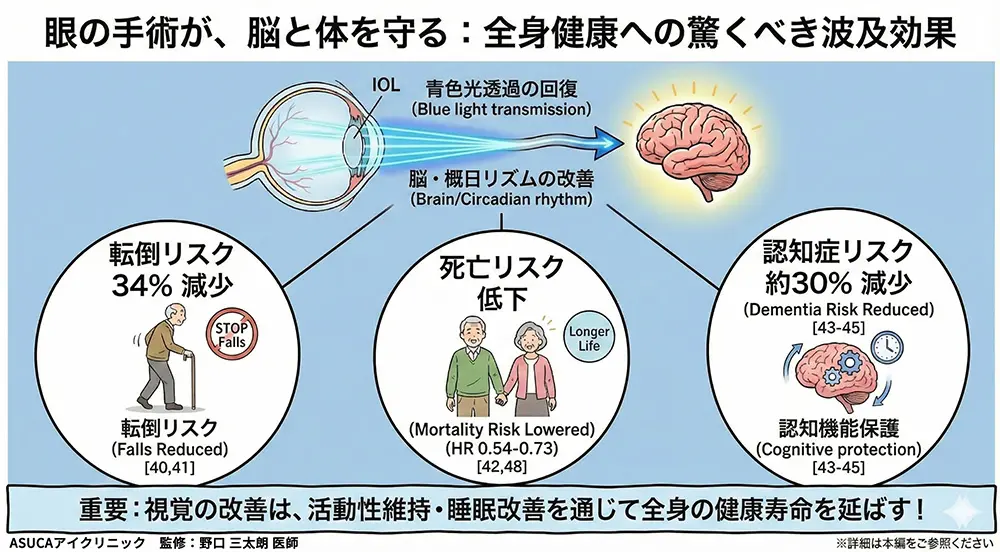
🏥7.転倒予防・認知症予防という驚きの効果
白内障手術の効果は「目」だけにとどまりません。体全体の健康にも大きな影響があることが、近年の大規模研究で明らかになっています。
🦴 転倒リスクが34%減少
70歳以上の女性306名を対象にしたランダム化比較試験で、白内障手術を受けた方は転倒する頻度が34%減ったことが報告されています[40,41]。高齢者の転倒は骨折→入院→寝たきりにつながるため、その予防効果は非常に大きな意味を持ちます。
🧠 認知症リスクが約29%低下
3,038名を長期追跡した研究で、白内障手術を受けた方は受けなかった方に比べて認知症の発症リスクが29%低いことが報告されました[43]。30万人を超える大規模コホート研究でも同様の結果が確認されています[44]。
2024年のメタ解析(558,276名のデータ統合)では約25%のリスク低下が報告されています[45]。
🧠 なぜ白内障手術で認知症が減る?
- 脳への視覚刺激が回復する
- 睡眠の質が良くなる(白内障は体内時計を乱す青色光をブロックしてしまう)[46,47]
- 外出や社会活動が増える
- 転倒への恐怖が減り運動量が維持される
💓 長期的な生存率の向上
白内障手術を受けた方は、受けなかった方と比較して長期死亡率が27~46%低いことが、複数の大規模研究で報告されています[42,48]。
📋8.こんなケースではどうする?具体例で解説
【ケースA】78歳男性 ── 進行した緑内障 + 中等度の白内障
- 矯正視力0.3、視野はかなり狭い
- 3種類の目薬を使って眼圧18 mmHg
- 「視野が狭いから手術しても意味がない」と言われていた
✅ 手術を行うべき理由
- 眼圧がさらに2〜4 mmHg下がり、点眼薬を減らせる可能性がある[16,17]
- OCTの画質が24%改善し、視神経の状態をより正確に評価できるようになる[24]
- 視野検査の精度が上がり、本当の進行が正確にわかるようになる[21,22]
- コントラスト改善による歩行安全性の向上で、転倒予防にもつながる[40]
【ケースB】82歳女性 ── 萎縮型の黄斑変性 + 後嚢下白内障
- 矯正視力0.1、中心暗点あり
- 「黄斑が萎縮しているので手術しても無駄」と説明されていた
✅ 手術を行うべき理由
- 最も進行した「中心性地図状萎縮」でも+4.4文字の有意な改善が得られている[27]
- 後嚢下白内障による強いまぶしさは手術で劇的に改善する[11,13]
- 黄斑変性の進行を加速させないことは大規模研究で確認済み[25]
- 認知症リスク29%低下、死亡率低下という全身的メリットが得られる[43,48]
【ケースC】65歳男性 ── 増殖糖尿病網膜症 + 成熟白内障
- 視力:手動弁(手の動きがかろうじてわかる程度)
- 白内障が進んで眼底が全く見えない状態
✅ 手術を行うべき理由
- 眼底が見えなければ、糖尿病網膜症のレーザー治療も注射治療もできない[31]
- 白内障手術は「治療のための前提条件」であり、手術しない=眼底疾患を放置すること
- 術中の抗VEGF注射で網膜症進行リスクを63%低減できる[36]
❓9.よくある質問
- 緑内障で視野が狭くなっていても、白内障手術を受ける意味はありますか?
- はい、大きな意味があります。白内障手術により眼圧が下がる効果(平均2.7~8.5 mmHg)が得られるほか、視野検査やOCTの精度が向上し、緑内障の正確な管理が可能になります。主要な国際ガイドライン(NICE, AAO, ESCRS)はいずれも、視力のみで手術適応を判断すべきではないとしています[5–7,16–24]。
- 加齢黄斑変性がありますが、白内障手術で病気が悪くなりませんか?
- AREDS2研究(4,553眼、最長10年追跡)で、白内障手術が黄斑変性を進行させないことが確認されています(HR 0.96; 95% CI 0.81–1.13)[25]。米国国立眼研究所(NEI)も「AMD悪化の懸念から白内障手術を回避する必要はない」と声明しています[26]。
- 糖尿病網膜症がある場合、白内障手術は危険ですか?
- 術後にやや進行するリスクはありますが、適切な周術期管理で大幅に軽減できます[36–39]。術中の抗VEGF注射で進行リスクを約63%低減できます。また、白内障があると眼底治療ができないため、白内障手術は治療の前提条件となるケースも多くあります[31]。
- 白内障手術で認知症が予防できるというのは本当ですか?
- 大規模コホート研究とメタ解析で一貫した結果が示されています。ACT Study(3,038名)では認知症リスクが29%低下(HR 0.71; P < 0.001)[43]、2024年メタ解析(55万人超)では約25%のリスク低下が報告[45]。視覚改善による脳刺激回復、概日リズム正常化、社会参加増加が関与すると考えられています。
- 視力がほとんど出ないほど網膜が悪くても、手術するメリットはありますか?
- あります。まぶしさの軽減・コントラスト改善は網膜の状態と独立に得られます[8,11,13,15]。さらに転倒リスク34%減少[40,41]、死亡率27~46%低下[42,48]、認知症リスク約25~29%低下[43–45]という全身的メリットは、最終視力に関係なく享受できます。
- 「視力だけで手術適応を決めてはいけない」というガイドラインはどこのものですか?
- 英国NICE(NG77, 2017年; 2025年再確認)が「視力のみを基準として手術アクセスを制限してはならない」と明記[5]。米国AAOも眼底可視化を独立した手術適応に認めており[6]、欧州ESCRS(2025年最新版)は認知健康効果を含め手術適応を広く認めています[7]。
📝【一般の方向け】まとめ
🌟 白内障手術の適応は「視力が良くなるかどうか」だけで決まるものではありません。
- ✅まぶしさの改善、コントラストの回復は、網膜・視神経の状態にかかわらず得られます
- ✅緑内障の管理に必要な検査精度が格段に向上します
- ✅黄斑変性の進行を加速させないことは大規模研究で証明済みです
- ✅糖尿病網膜症の治療には、まず白内障を除去する必要があるケースが多い
- ✅転倒予防(34%減少)、認知症予防(約25~29%低下)、生存率向上(HR 0.54~0.73)も享受できます
「どうせ見えないから」ではなく、「手術しないことで何を失うか」を考えることが大切です。
目の奥の病気があるから手術できないのではなく、目の奥の病気があるからこそ手術が必要なケースが多いのです。
🏥 当院での取り組み
ASUCAアイクリニック仙台マークワンでは、白内障手術と網膜硝子体手術の両方に対応しています。緑内障・加齢黄斑変性・糖尿病網膜症を合併した白内障に対しても、精密な術前検査と周術期管理を行い、安全かつ最大限の効果を追求しています。
「自分の場合、手術した方がいいのだろうか?」と迷われている方は、一度ご相談ください。
執筆者(野口三太朗医師)への診察予約・お問い合わせは、記事の最後にご案内しています。
🔬 眼科医・専門家向け
── ここから先は眼科医・医療従事者向けの専門的な解説です ──
📐11.光学物理学的根拠
光学物理学的根拠:CSF分解定理とストレイライト
コントラスト感度関数(CSF)の分解定理
Campbell & Green(1965年)の古典的研究に端を発し、Michaelら(Acta Ophthalmologica, 2011年)[8]の臨床検証によって確立された基本定理を以下に示す。
CSF分解定理(CSF Decomposition Theorem)
CSFtotal(u) = MTFoptical(u) × CSFneural(u)
CSFtotal(u):測定される全体のコントラスト感度(患者が体験する視覚の質)
MTFoptical(u):眼光学系の変調伝達関数(角膜〜水晶体〜硝子体の透明度と収差に依存)
CSFneural(u):網膜〜視神経〜視覚皮質による神経処理コントラスト感度
u:空間周波数(cycles per degree: cpd)
📐 高校数学で理解するポイント
改善率 = (MTFnew × CSFneural) ÷ (MTFold × CSFneural) = MTFnew / MTFold。分子と分母のCSFneuralが約分されるため、網膜の状態は改善率に一切影響しない。MTFopticalが0.35→0.95に回復した場合、改善率は常に約2.7倍であり、健常眼でも重度視神経萎縮眼でも同値。
乗法モデルに基づく白内障手術の視機能改善シミュレーション
| 病態 | MTFopt(術前) | CSFneural | CSFtotal(術前) | MTFopt(術後) | CSFtotal(術後) | 改善率 |
|---|---|---|---|---|---|---|
| 健常眼+白内障 | 0.35 | 1.00 | 0.35 | 0.95 | 0.95 | 2.7倍 |
| 軽度緑内障+白内障 | 0.35 | 0.70 | 0.245 | 0.95 | 0.665 | 2.7倍 |
| 中等度AMD+白内障 | 0.35 | 0.45 | 0.158 | 0.95 | 0.428 | 2.7倍 |
| 高度DR+白内障 | 0.35 | 0.25 | 0.088 | 0.95 | 0.238 | 2.7倍 |
| 重度視神経萎縮+白内障 | 0.35 | 0.10 | 0.035 | 0.95 | 0.095 | 2.7倍 |
💡 眼内散乱光(ストレイライト)
散乱光パラメータの定義[9,10]
log(s) = log[ θ² × PSF(θ) ] (θ = 7°で評価)
s:散乱角θにおけるPSFの強度にθ²を掛けた値
PSF(θ):点光源像の広がりを表す関数
年齢依存の正常散乱光値(Rozema et al., IOVS 2010)[10]
log(s) = 0.87 + log[ 1 + (Age / 65)⁴ ]
📐 高校数学で理解するポイント
(Age/65)⁴の4乗項は65歳を超えると急速に増大。40歳→0.14、65歳→1.0、80歳→2.29と加速度的に増大し、白内障はこの値をさらに押し上げる。
白内障形態別の散乱光パラメータ log(s)[11]
| 白内障の形態 | log(s)(±SD) | 正常との差 | 視力との相関(R²) |
|---|---|---|---|
| 正常若年眼 | 0.90 ± 0.10 | —(基準) | — |
| 核白内障 | 1.22 ± 0.20 | +0.32 | 0.34 |
| 皮質白内障 | 1.26 ± 0.23 | +0.36 | 0.21 |
| 後嚢下白内障(PSC) | 1.48 ± 0.34 | +0.58 | 0.13 |
PSCでは視力との相関がR² = 0.13(r ≈ 0.36)にすぎない。OSI(Objective Scatter Index)はダブルパス法による客観的光学指標であり、< 1.0正常、3.0–7.0手術適応に対応する[14]。Vingopoulosら(Harvard/Mass Eye and Ear, 2022年)[15]は、偽水晶体眼のAULCSFが1.053→1.256へ回復し年齢対照群と同等であることを示した。
💧12.緑内障:IOP・視野・OCTの三重メリット
眼圧低下の定量的エビデンス
| 研究 | 対象 | 平均IOP下降 | 下降率 | 追跡期間 | 出典 |
|---|---|---|---|---|---|
| Mansberger (OHTS) | 高眼圧症 743眼 | −4.1 mmHg | 16.5% | ≥36ヶ月 | [16] |
| Poley et al. | OAG(BL 23–29) | −8.5 mmHg | 34% | 最長10年 | [17] |
| Poley et al. | OAG(BL 15–17) | −1.1 mmHg | 〜7% | 最長10年 | [17] |
| Latina (meta) | 開放隅角 | −2.7〜−3.8 | — | 12ヶ月 | [18] |
| Latina (meta) | 閉塞隅角 | −6.4〜−9.5 | 30–35% | 12–36ヶ月 | [18] |
| EAGLE (RCT) | 原発閉塞隅角 | LPIより1.18低値 | — | 3年 | [19] |
Poleyらの用量反応関係[17]が注目に値する。ベースラインIOPが高いほど術後下降幅が大きく、水晶体厚と前房容積の関係から生理学的に説明可能。EAGLE trial[19]は閉塞隅角緑内障においてclear lens extractionを第一選択として確立し、LPI群と比較して追加治療要のリスクをOR 10.1倍低く抑えた。
視野検査精度の向上
Kouchekiら(AJO, 2004年; AGIS data, 158眼)[21]は、白内障術後にMDが+1.3 dB改善(P ≤ 0.001)する一方、PSDがわずかに悪化することを報告。びまん性光量低下の除去により局所欠損が鮮明化された結果と解釈される。Smith, Katz & Quigley[22]もMD +1.68 dBの改善を確認。Seolら[23]はPSCが視野アーティファクトに最大の影響を与えることを特定した。
OCT画像品質の改善
Mwanzaら(J Glaucoma, 2011年)[24]は、白内障術後にOCTシグナル強度が平均24.1%上昇(P < 0.001)、測定RNFL厚が9.3%増加(P = 0.001)することを示した。術前シグナル > 6の眼ではRNFL厚に有意変化なし(P = 0.14)であり、白内障によるアーティファクトがRNFL菲薄化を偽装し得ることが確認された。
| パラメータ | 術前の問題 | 術後の改善 | 臨床的意義 |
|---|---|---|---|
| VF MD | びまん性感度低下 | +1.3〜+1.68 dB[21,22] | 新BL確立 |
| VF PSD | 偽低値 | わずかに上昇[21] | 局所欠損の鮮明化 |
| OCTシグナル | 信号減衰 | +24.1%[24] | 測定信頼性向上 |
| RNFL厚 | 偽菲薄化 | +9.3%[24] | 進行誤判定の防止 |
| IOP | 薬物負荷 | −2.7〜−9.5 mmHg[16–19] | 減薬の可能性 |
🔍 13.AMD:AREDS2が示した安全性と視力改善
AMD進行リスク:AREDS2 Report No. 27
4,553眼を最長10年追跡したAREDS2 Report No. 27(Bhandariら, Ophthalmology, 2022年)[25]は、白内障手術と晩期AMD進行との間に有意な関連を認めなかった。
| 解析方法 | HR/OR | 95% CI | 解釈 |
|---|---|---|---|
| 右眼 time-to-event | HR 0.96 | 0.81–1.13 | リスク増加なし |
| 左眼 time-to-event | HR 1.05 | 0.89–1.25 | リスク増加なし |
| Matched-pair | OR 0.92 | 0.77–1.10 | リスク増加なし |
AMD重症度別の術後視力改善
| AMD重症度 | 平均改善(ETDRS文字) | 95% CI | P値 |
|---|---|---|---|
| 🟢 軽度 | +11.2 | 6.9–15.5 | < 0.0001 |
| 🟡 中等度 | +11.1 | 9.1–13.2 | < 0.0001 |
| 🟠 高度 | +8.7 | 6.7–10.7 | < 0.0001 |
| 非中心性 GA | +8.9 | 5.8–12.1 | < 0.0001 |
| 血管新生型 | +7.5 | 有意 | < 0.0001 |
| 中心性 GA | +4.4 | 有意 | 0.005 |
Taipaleら[28]は重度両眼性AMD患者のNEI VFQ-25複合スコアが44.0→56.9(P=0.045)に改善と報告。Lamoureuxら[29]はRCTで早期手術群のQOLに中〜大効果量(Cohen’s d = 0.66–0.91)を確認。Kesselら[30]は抗VEGF治療中nAMDで術後+7.1 ETDRS文字改善・注射頻度に差なし(1.5 vs 1.7回/6ヶ月)を報告。
💉14.DR:治療アクセスと周術期リスク管理
NICE 2024年エビデンスレビュー[31]は「白内障の存在は一般に、レーザーが網膜の正しい領域をターゲットできないことを意味する」と明記。Mittraら[32]は150眼で≧2段階VA改善78%・20/40以上62%を報告。Ostriら[33]もDR全カテゴリーで有意なCDVA改善を確認。
Leeら(AJO, 2024; meta, 15研究, 7,287患者)[34]はDR進行 RR 1.46(1.28–1.66)、STDR RR 1.84(1.21–2.81)を報告。Dennistonら(BJO, 2017; UK DR EMR, 4,850眼)[35]は治療要DMEが術前2.9%→術後5.3%に上昇と報告。
| 戦略 | エビデンス | 効果量 | 出典 |
|---|---|---|---|
| 術中/術前 抗VEGF | meta(Wang 2024) | RR 0.37(0.19–0.70) | [36] |
| ネパフェナク90日TID | RCT(Singh 2012; 263眼) | ME 16.7%→3.2% | [37] |
| 術前1週間の抗VEGF | 比較(Güven 2025) | CMT上昇なし(P=0.948) | [38] |
| 活動性増殖病変の事前治療 | SR(Kelkar 2018) | 合併症リスク低減 | [39] |
⚠️ IOL選択の注意点
Kelkarら[39]はDR合併眼では単焦点IOLを第一選択とすべきと強調する。多焦点IOLは眼底可視化を阻害しレーザー光凝固精度を低下させる。
🧠15.全身的アウトカム
転倒リスク低減
Harwoodら(BJO, 2005; RCT, ≥70歳女性306名)[40]は迅速化白内障手術により転倒率34%低減を実証。2021年SR/MA[41]も同効果量を確認。
長期死亡率
| 研究 | 対象 | 調整後HR | 95% CI |
|---|---|---|---|
| Fong 2013(Blue Mountains) | 354名, 15年 | 0.54 | 0.41–0.73 |
| Tseng 2016(US Medicare) | 150万人 | 0.73 | 0.72–0.74 |
認知症リスク低減
| 研究 | デザイン・対象 | 主要結果 | 出典 |
|---|---|---|---|
| Lee 2022(ACT) | 前向きコホート, 3,038名 | 認知症 HR 0.71(0.62–0.83) 緑内障手術 HR 1.08(n.s.)→負の対照 | [43] |
| Ma 2023(UK Biobank) | 300,823名 | 未治療白内障: HR 1.21(認知症), 1.48(AD) 手術群: 健常対照と有意差なし | [44] |
| 2024 meta | 24文献, 558,276名 | HR 0.75(0.72–0.78) | [45] |
🔬 因果推論の強化
Leeらの研究で緑内障手術が認知症と無関連(HR 1.08, P = 0.68)であった点が負の対照として機能し、白内障手術固有の光学系改善→認知保護経路を支持する[43]。
概日リズムと睡眠
Brøndstedら(Ophthalmology, 2015; RCT)[46]は、白内障手術により青色光瞳孔反応17–24%↑、メラトニンピーク上昇(P=0.037)、概日リズム22分前進(P=0.004)を示した。メタ解析[47]はPSQI改善 MD = −0.62(P=0.02)を確認。水晶体の黄色化がipRGCのメラノプシン色素(λmax ≈ 480 nm)への有効照度を低下させ、SCN光同調を障害する機序が提唱されている。
| メカニズム | エビデンス | 出典 |
|---|---|---|
| 感覚遮断の解除(”use it or lose it”) | 視覚入力低下→視覚野不活動→神経変性促進。手術で連鎖を断つ | [43,46] |
| 青色光透過回復・概日リズム正常化 | RCT: 青色光瞳孔反応17–24%↑、メラトニン↑、リズム22分前進 | [46] |
| 睡眠の質改善 | MA: PSQI MD = −0.62(P=0.02) | [47] |
| 社会的孤立・うつの軽減 | 視覚改善→外出増加→社会参加→認知予備力維持 | [43,45] |
| 身体活動の維持 | 転倒恐怖軽減→運動継続→認知症予防因子 | [40,41] |
📋16.国際ガイドラインの立場
| ガイドライン | 主要記載 | エビデンスレベル | 出典 |
|---|---|---|---|
| NICE NG77(2017, 2025再確認) | 「視力のみを基準として白内障手術へのアクセスを制限してはならない」。QOLへの影響で判断。 | 推奨(強) | [5] |
| AAO PPP(Miller 2022) | 「眼底を観察するために必要な場合」を手術適応に明記(A:III)。 | A:III | [6] |
| ESCRS(2025年9月) | 「白内障手術は緑内障、DR、AMDの管理を促進」。認知健康効果を認定。 | GRADE +/++ | [7] |
| RCOphth(2010) | 「後眼部疾患の治療・モニタリング促進」を手術適応に記載。 | 推奨 | [49] |
| ICO | AAOに準拠。眼底可視化の必要性を適応として認定。 | — | [50] |
📝【眼科医向け】まとめ
後眼部疾患合併眼における白内障手術のエビデンスは、Snellen視力を超えた多層的な臨床的意義を有する。
CSF = MTFoptical × CSFneuralの乗法モデルは、光学系改善の相対的利益がCSFneuralに依存しないことを数学的に証明する。IOP降下効果(最大−9.5 mmHg)は緑内障管理に直結し、VF/OCTの精度向上は疾患モニタリングの根幹を支える。AREDS2はAMD進行を加速させないことを確証し、DRリスクは周術期管理で大幅軽減される。転倒34%減少(RCT)、死亡率HR 0.54–0.73、認知症HR 0.71–0.75の全身的恩恵は最終VAが限定的でも発現し得る。
問われるべきは「手術して視力が出るか」ではなく、「手術しないことで何を失うか」である。
📚 参考文献
1. [1] Lamoureux EL, et al. The impact of cataract surgery on quality of life. Curr Opin Ophthalmol. 2011;22(1):19–27. https://pubmed.ncbi.nlm.nih.gov/21088580/
2. [2] Harwood RH, et al. Falls and health status in elderly women following first eye cataract surgery: an RCT. BJO. 2005;89(1):53–59. https://pmc.ncbi.nlm.nih.gov/articles/PMC1772474/
3. [3] Lee CS, et al. Association between cataract extraction and development of dementia. JAMA Intern Med. 2022;182(2):134–141. https://pubmed.ncbi.nlm.nih.gov/34870676/
4. [4] Mansberger SL, et al. Reduction in IOP after cataract extraction: the OHTS. Ophthalmology. 2012;119(9):1826–1831. https://pmc.ncbi.nlm.nih.gov/articles/PMC3426647/
5. [5] NICE. Cataracts in adults: management (NG77). 2017 (reaffirmed 2025). https://www.nice.org.uk/guidance/ng77
6. [6] Miller KM, et al. Cataract in the Adult Eye PPP. Ophthalmology. 2022;129(1):P1–P126. https://www.aao.org/preferred-practice-pattern/cataract-in-adult-eye-ppp
7. [7] ESCRS Guideline for Cataract Surgery. Sept 2025. https://www.escrs.org/escrs-guideline-for-cataract-surgery/
8. [8] Michael R, et al. Neural contrast sensitivity calculated from measured total CS and MTF. Acta Ophthalmol. 2011;89(3):e234–e239. https://pubmed.ncbi.nlm.nih.gov/19909292/
9. [9] van den Berg TJTP, et al. Straylight effects with aging and lens extraction. AJO. 2007;144(3):358–363. https://pubmed.ncbi.nlm.nih.gov/17631847/
10. [10] Rozema JJ, et al. Retinal straylight as a function of age and ocular biometry. IOVS. 2010;51(5):2795–2799. https://iovs.arvojournals.org/article.aspx?articleid=2186495
11. [11] Gholami S, et al. Changes in intraocular straylight and VA with age in cataracts of different morphologies. J Ophthalmol. 2017;2017:5649532. https://pmc.ncbi.nlm.nih.gov/articles/PMC5554999/
12. [12] Seol BR, et al. Changes of VF global indices after cataract surgery in POAG patients. Jpn J Ophthalmol. 2016;60(6):439–445. https://pubmed.ncbi.nlm.nih.gov/27503400/
13. [13] Reus NJ, van den Berg TJTP. Changes in straylight after cataract surgery. JCRS. 2024;50(2):148–153. https://pmc.ncbi.nlm.nih.gov/articles/PMC10878460/
14. [14] Artal P, et al. An objective scatter index based on double-pass retinal images to classify cataracts. PLoS ONE. 2011;6(2):e16823. https://pubmed.ncbi.nlm.nih.gov/21347228/
15. [15] Vingopoulos F, et al. Active learning to characterize the full CSF in cataracts. Clin Ophthalmol. 2022;16:3109–3118. https://pmc.ncbi.nlm.nih.gov/articles/PMC9509679/
16. [16] Mansberger SL, et al. Reduction in IOP after cataract extraction: the OHTS. Ophthalmology. 2012;119(9):1826–1831. https://pmc.ncbi.nlm.nih.gov/articles/PMC3426647/
17. [17] Poley BJ, et al. IOP reduction after phacoemulsification with IOL in glaucomatous and nonglaucomatous eyes. JCRS. 2009;35(11):1946–1955. https://pubmed.ncbi.nlm.nih.gov/19878828/
18. [18] Latina MA, et al. The role of phacoemulsification in glaucoma therapy: SR and MA. Surv Ophthalmol. 2017;62(5):676–690. https://www.sciencedirect.com/science/article/abs/pii/S003962571730108X
19. [19] Azuara-Blanco A, et al. Effectiveness of early lens extraction for PACG (EAGLE). Lancet. 2016;388(10052):1389–1397. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(16)30956-4/fulltext
20. [20] Saunders LJ, et al. Visual field testing for glaucoma. Community Eye Health. 2012;25(79-80):66–70. https://pmc.ncbi.nlm.nih.gov/articles/PMC3588129/
21. [21] Koucheki B, et al. Visual field changes after cataract extraction: the AGIS experience. AJO. 2004;138(6):1022–1028. https://pubmed.ncbi.nlm.nih.gov/15629295/
22. [22] Smith SD, Katz J, Quigley HA. Effect of cataract extraction on automated perimetry in glaucoma. Arch Ophthalmol. 1997;115(12):1515–1519. https://pubmed.ncbi.nlm.nih.gov/9400784/
23. [23] Seol BR, et al. Changes of VF global indices after cataract surgery in POAG. Jpn J Ophthalmol. 2016;60(6):439–445. https://pubmed.ncbi.nlm.nih.gov/27503400/
24. [24] Mwanza JC, et al. Effect of cataract and its removal on signal strength and RNFL OCT measurements. J Glaucoma. 2011;20(1):37–43. https://pubmed.ncbi.nlm.nih.gov/20179622/
25. [25] Bhandari S, et al. Cataract surgery and risk of late AMD: AREDS2 Report No. 27. Ophthalmology. 2022;129(4):414–420. https://www.sciencedirect.com/science/article/abs/pii/S0161642021009015
26. [26] NEI. Cataract surgery does not cause disease progression in people with AMD. 2021. https://www.nei.nih.gov/about/news-and-events/news/cataract-surgery-does-not-cause-disease-progression-people-amd
27. [27] Huynh N, et al. VA after cataract surgery in patients with AMD: AREDS2 Report No. 5. Ophthalmology. 2014;121(6):1229–1236. https://pubmed.ncbi.nlm.nih.gov/24613825/
28. [28] Taipale C, et al. Effect of cataract surgery on QOL in patients with severe VI due to AMD. Ann Transl Med. 2020;8(22):1543. https://atm.amegroups.org/article/view/43437/html
29. [29] Lamoureux EL, et al. Impact of cataract surgery on QOL in patients with early AMD. Optom Vis Sci. 2007;84(8):683–688. https://pubmed.ncbi.nlm.nih.gov/17700333/
30. [30] Kessel L, et al. Cataract surgery in patients with neovascular AMD. Acta Ophthalmol. 2016;94(8):755–760. https://pubmed.ncbi.nlm.nih.gov/27255691/
31. [31] NICE. Evidence review for treatments before/during/after cataract surgery for DR/DMO. 2024. https://www.ncbi.nlm.nih.gov/books/NBK607258/
32. [32] Mittra RA, et al. Retinopathy progression and visual outcomes after phaco in DM. Arch Ophthalmol. 2000;118(7):912–917. https://pubmed.ncbi.nlm.nih.gov/10900103/
33. [33] Ostri C, et al. Phacoemulsification in a large cohort of diabetes patients. JCRS. 2011;37(11):2006–2012. https://www.sciencedirect.com/science/article/abs/pii/S0886335011011758
34. [34] Lee JY, et al. Incidence and progression of DR after cataract surgery: SR and MA. AJO. 2024;264:87–97. https://www.sciencedirect.com/science/article/abs/pii/S0002939424003799
35. [35] Denniston AK, et al. UK DR EMR Report 2: impact of cataract surgery on DMO. BJO. 2017;101(12):1673–1678. https://pubmed.ncbi.nlm.nih.gov/28487377/
36. [36] Wang Y, et al. Management after cataract surgery for DR: SR and MA. Int Ophthalmol. 2024;44:163. https://pubmed.ncbi.nlm.nih.gov/38557801/
37. [37] Singh R, et al. Nepafenac in prevention of ME following cataract surgery in DR. Clin Ophthalmol. 2012;6:1259–1269. https://pubmed.ncbi.nlm.nih.gov/22927737/
38. [38] Güven D, et al. Phaco in patients with DME: anti-VEGF before or simultaneously? Int J Ophthalmol. 2025;18(3):432–439. https://pmc.ncbi.nlm.nih.gov/articles/PMC11947536/
39. [39] Kelkar A, et al. Cataract surgery in diabetes mellitus: SR. Indian J Ophthalmol. 2018;66(10):1401–1410. https://pmc.ncbi.nlm.nih.gov/articles/PMC6173035/
40. [40] Harwood RH, et al. Falls and health status following first eye cataract surgery: RCT. BJO. 2005;89(1):53–59. https://pmc.ncbi.nlm.nih.gov/articles/PMC1772474/
41. [41] Gutiérrez-Robledo LM, et al. Cataract surgery and falls: SR and MA. J Ophthalmol. 2021;2021:2983680. https://pubmed.ncbi.nlm.nih.gov/33815834/
42. [42] Tseng VL, et al. Cataract surgery and mortality in US Medicare. Ophthalmology. 2016;123(5):1019–1026. https://www.aaojournal.org/article/S0161-6420(15)01557-2/abstract
43. [43] Lee CS, et al. Cataract extraction and dementia. JAMA Intern Med. 2022;182(2):134–141. https://pubmed.ncbi.nlm.nih.gov/34870676/
44. [44] Ma LZ, et al. Cataract, cataract surgery, and risk of dementia. Biol Psychiatry. 2023;93(9):810–819. https://pubmed.ncbi.nlm.nih.gov/35940935/
45. [45] Yuan M, et al. Cataract surgery and cognitive benefits: SR and MA. Ophthalmology. 2024;131(8):920–931. https://pubmed.ncbi.nlm.nih.gov/38336283/
46. [46] Brøndsted AE, et al. Cataract surgery and circadian photoentrainment: RCT. Ophthalmology. 2015;122(10):2115–2124. https://pubmed.ncbi.nlm.nih.gov/26233628/
47. [47] Zheng Y, et al. Cataract surgery and sleep quality: SR and MA. Int J Ophthalmol. 2017;10(11):1734–1741. https://pubmed.ncbi.nlm.nih.gov/29181319/
48. [48] Fong CSU, et al. Correction of VI by cataract surgery and improved survival: Blue Mountains Eye Study. Ophthalmology. 2013;120(9):1720–1727. https://pubmed.ncbi.nlm.nih.gov/23664468/
49. [49] Royal College of Ophthalmologists. Cataract Surgery Guidelines. 2010. https://curriculum.rcophth.ac.uk/wp-content/uploads/2014/12/2010-SCI-069-Cataract-Surgery-Guidelines-2010-SEPTEMBER-2010-1.pdf
50. [50] ICO. International Clinical Guidelines: Cataract. http://www.todnet.org/toddata/seminerler/ICOClinicalGuidelines.pdf
本記事は2024年までの英語査読付き文献エビデンスに基づいて作成されました。個々の病態や治療方針については、必ず眼科専門医にご相談ください。
ASUCAアイクリニック 仙台マークワンは、白内障手術(眼内レンズ手術)、硝子体手術、ICL・IPCL、目の周りやまぶたなどを治療する手術専門クリニックです。
当院は、一人ひとりに精密な検査と時間を確保するため、完全予約制としております。
予約のページから予約の上お越しください。
ご不明な点がございましたら、LINEやお問い合わせページにて対応しております。
アクセス
宮城県仙台市青葉区中央一丁目2-3 仙台マークワン11F
仙台駅直結徒歩2分
*県外から当院で自費手術を受けられる方を対象とした「交通費負担軽減制度(手術代金より1万円の充当)」を設けております。詳細はスタッフにお問い合わせください。
免責事項本記事は教育・情報提供を目的としており、個別の医療相談や診断・治療の代替となるものではありません。眼科治療を検討される場合は、必ず眼科専門医にご相談ください。医学情報は日々更新されるため、最新情報の確認も重要です。