新しいIOLが常に優れているわけではない🔬 EDOF・多焦点眼内レンズの光学的真実と臨床評価の盲点
🎯 この記事のポイント
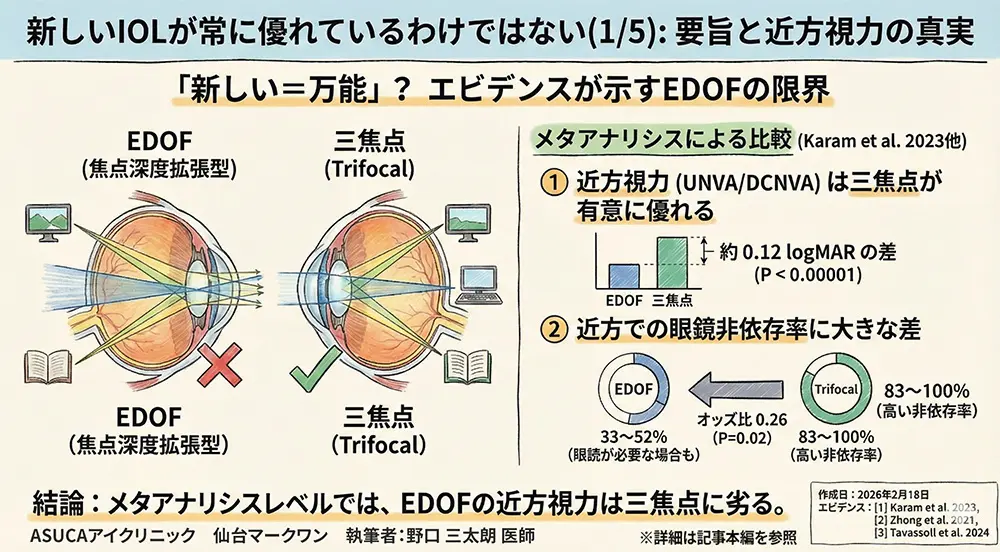
- ✅EDOF(焦点深度拡張型)レンズは三焦点IOLの「進化形」ではなく、近方視力と眼鏡非依存率で明確に劣る——メタアナリシス(22研究・2,200眼)が一貫して示すエビデンスです
- ✅「EDOFはハロー・グレアが少ない」は科学的に支持されていない——Cochrane系統的レビューでも有意差なしと結論
- ✅大切なのは「新しさ」ではなく、あなたの生活スタイルに合ったレンズ選び——物理法則上、万能レンズは存在しません
- 🔰 1. そもそもEDOFレンズって何?
- 📊 2. EDOFレンズと三焦点レンズ、何が違うの?
- 🌙 3. 「EDOFはハロー・グレアが少ない」って本当?
- 🏠 4. あなたに合ったレンズの選び方
- ❓ よくある質問(FAQ)
- 📝 一般の方向けまとめ
- 👨⚕️ 眼科医・医療従事者の方へ——エビデンスに基づくIOL光学性能の詳細検証
- 📚 1. メタアナリシスが示すEDOFの近方視力の限界
- 📈 2. デフォーカスカーブが暴く焦点範囲の真実
- ⚛️ 3. IOL光学設計の物理学:回折・屈折・色収差の数理
- 🔬 4. Through-focus MTFとStrehl比:光学ベンチが示す不都合な真実
- 🌟 5. ハロー・グレアにおけるEDOF優位の神話
- ⚠️ 6. 見落とされる評価指標:なぜ多くの眼科医がIOLの真の性能を把握できないのか
- 🎯 7. 結論:エビデンスに基づくIOL選択と評価の転換
- 📖 参考文献
👁️ 一般の患者さんへ——白内障手術のレンズ選びで後悔しないために
ここでは、難しい専門用語をなるべく使わず、白内障手術を検討されている患者さんに向けて、レンズ選びの大切なポイントをわかりやすくお伝えします。
🔰 1. そもそもEDOFレンズって何?
白内障手術では、濁った水晶体の代わりに眼内レンズ(IOL)を目の中に入れます。このレンズにはいくつかの種類があります。
- 単焦点レンズ:遠くまたは近くのどちらか一方にピントが合う、最も基本的なレンズ
- 多焦点レンズ(三焦点IOL):遠く・中間・近くの3つの距離にピントが合うよう設計されたレンズ(例:PanOptix、FineVisionなど)
- EDOFレンズ(焦点深度拡張型):ピントの合う範囲を「広げる」ことを目指したレンズ(例:Symfony、Vivityなど)
EDOFは「Extended Depth of Focus(焦点深度拡張)」の略で、遠くから中間距離まで自然に見えることを目指した設計です。比較的新しいタイプのレンズであるため、「新しい=優れている」と思われがちですが、実はそう単純ではありません。
📊 2. EDOFレンズと三焦点レンズ、何が違うの?
大規模な医学研究(22件の研究、2,200眼以上を統合した分析)から、以下のことが明らかになっています[1][2][3]。
📋わかりやすい比較表
| 見え方のポイント | EDOFレンズ | 三焦点レンズ | 結果 |
|---|---|---|---|
| 🚗 遠くの見え方(運転など) | ◎ よく見える | ◎ よく見える | 差なし |
| 💻 中間距離(パソコンなど) | ◎ よく見える | ◎ よく見える | ほぼ差なし |
| 📖 近くの見え方(読書・スマホ) | △ やや見にくい | ◎ よく見える | 三焦点が明確に優位 |
| 👓 近方で眼鏡なしでOKな割合 | 33〜52% | 83〜100% | 三焦点が大幅に優位 |
| 🌙 夜の光のにじみ(ハロー・グレア) | 同程度 | 同程度 | 差なし |
| 😊 患者さんの満足度 | 高い | 高い | 差なし |
💡 ここがポイント
EDOFレンズは遠くから中間距離まではとてもよく見えますが、近く(読書・スマホ・新聞など)の見え方では三焦点レンズに劣ることが、多くの信頼性の高い研究で確認されています。EDOFレンズを選んだ方の約半数は、近くを見るときに眼鏡が必要になるのに対し、三焦点レンズでは8割以上の方が近くも眼鏡なしで生活できています[1][10]。
🌙 3. 「EDOFはハロー・グレアが少ない」って本当?
ハロー(光の周りに輪が見える現象)やグレア(まぶしさ)は、多焦点レンズの代表的な副作用です。「EDOFレンズはこうした光の副作用が少ない」と説明されることがありますが、これは最新のエビデンスでは支持されていません。
- 🔍 2023年の大規模メタアナリシス(22研究・2,200眼):EDOFと三焦点でハロー・グレアに有意差なし[1]
- 🔍 2024年のCochrane系統的レビュー(最も厳格な医学評価):ハロー・グレアに臨床的に意味のある差なし[3]
- 🔍 客観的測定(Light Distortion Analyzer)でも:EDOFの光の散乱は三焦点と同等ないしそれ以上という報告あり[13]
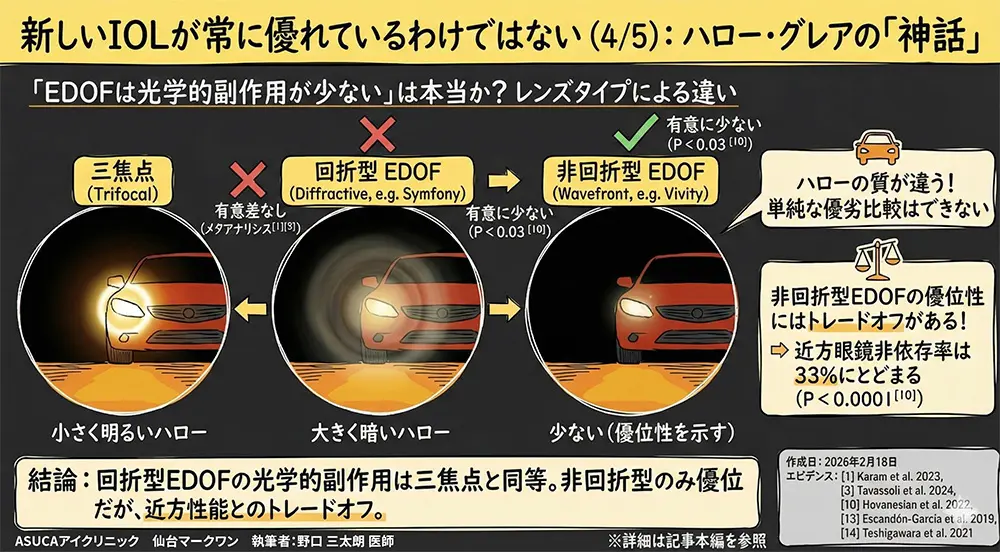
ただし、非回折型EDOF(Vivityなど)に限っては、ハロー・グレアが少ないという報告があります[10]。しかし、その代わりに近くの見え方は大幅に犠牲になり、完全な眼鏡非依存率はわずか33%(三焦点PanOptixの83%に対して)です[10]。
⚖️ つまり、こういうことです
どのレンズにも「良い面」と「代償」があります。物理法則上、ピントが合う範囲を広げれば光の質は下がり、光の質を優先すればピントの範囲は狭くなります。「すべてが完璧なレンズ」は存在しないのです。
🏠 4. あなたに合ったレンズの選び方
最も大切なのは、あなたの日常生活でどの距離を最も重視するかです。
🎯 レンズ選びのチェックリスト
- 📖 読書・スマホ・手芸など近くの作業を眼鏡なしでしたい → 三焦点レンズが向いています
- 🚗 夜間の運転が多く、光のにじみが心配 → 非回折型EDOF(Vivity等)が選択肢に(ただし近方は眼鏡が必要になりやすい)
- 💻 パソコン作業が中心で、近くは眼鏡でもOK → EDOFレンズも良い選択肢です
- 🔭 とにかく遠くがクリアに見えることが最優先 → 単焦点レンズが最も高い光学品質を提供します
⚠️ 受診前にぜひ準備してほしいこと
- 📝 1日の過ごし方を書き出してみてください(どの距離をよく見るか)
- 👓 眼鏡をかけてもいい場面と絶対に眼鏡をかけたくない場面を整理しましょう
- 🌙 夜間の運転をするかどうかも重要なポイントです
- ❓ デフォーカスカーブ(各距離での見え方のグラフ)を見せてもらえるか聞いてみましょう
当院では、患者さん一人ひとりの生活スタイルを詳しくお聞きしたうえで、デフォーカスカーブ・コントラスト感度・ハロメトリーなど複数の客観的データをお見せしながら、最適なレンズを一緒に選んでいます。「新しいから良い」ではなく、「あなたに合っているから良い」——これが当院のレンズ選びの基本方針です。
❓ よくある質問(FAQ)
- EDOFレンズと三焦点レンズ、どちらが良いですか?
- どちらが「良い」かは患者さんのライフスタイルによります。近くの作業(読書・スマホ)を眼鏡なしで行いたい方には三焦点IOLが適しています(眼鏡不要率83〜100%)。一方、夜間運転が多く光のにじみを最小限にしたい方には非回折型EDOF(Vivityなど)が選択肢になりますが、近方で眼鏡が必要になる可能性が高くなります(眼鏡不要率33〜52%)。
- EDOFレンズはハロー・グレアが少ないと聞きましたが本当ですか?
- 複数のメタアナリシスおよびCochrane系統的レビューでは、回折型EDOF(Symfony)と三焦点IOLの間にハロー・グレアの統計的有意差は認められていません[1][3]。非回折型EDOF(Vivity)ではハロー・グレアの軽減が報告されていますが、その代わり近方視力と眼鏡非依存率が大きく低下します[10]。
- EDOFレンズで近くが見えにくくなることはありますか?
- はい。メタアナリシスのデータでは、EDOFレンズは三焦点IOLと比較して近方視力が約0.12 logMAR(約1行分)劣ります[1]。FDA承認前データでは、両眼で近方20/20以上を達成できた割合はSymfony 22%に対し、PanOptix 50%でした[9]。EDOFレンズの方には近方用の眼鏡が必要になる可能性があります。
- 新しいレンズほど性能が良いのですか?
- 必ずしもそうではありません。EDOFレンズは三焦点IOLの「進化形」ではなく、異なるトレードオフを持つ設計です。物理法則上、広い焦点範囲と高いピークコントラストを同時に達成することは不可能であり、どのレンズにも長所と短所があります。重要なのは患者さん一人ひとりの生活スタイルに合ったレンズを選ぶことです。
- 白内障手術で使う眼内レンズはどうやって選べばいいですか?
- まず日常生活で最も重視する距離(遠方・中間・近方)を整理し、眼鏡を使ってもよい場面とそうでない場面を明確にしましょう。そのうえで、担当の眼科医にデフォーカスカーブやコントラスト感度などの客観的データを基にした説明を受け、ご自身に最適なレンズを一緒に決めることが大切です。
📝 一般の方向けまとめ
- ✅ EDOFレンズは遠く〜中間はよく見えるが、近くの見え方と眼鏡からの解放度では三焦点に劣る
- ✅ 「EDOFはハロー・グレアが少ない」は回折型では科学的に支持されていない
- ✅ 万能レンズは存在しない——大切なのはあなたのライフスタイルに合った選択
- ✅ レンズ選びはデフォーカスカーブなどの客観的データに基づいて行うべき
- ✅ 迷ったら、複数の指標で丁寧に説明してくれる眼科を選びましょう
執筆者(野口三太朗医師)への診察予約・お問い合わせは、記事の最後にご案内しています。
📞 白内障手術のレンズ選びでお悩みの方は、お気軽にご相談ください。
👨⚕️ 眼科医・医療従事者の方へ——エビデンスに基づくIOL光学性能の詳細検証
以下は、眼科医および医療従事者を対象とした専門的内容です。査読付き英語論文のエビデンスに基づき、EDOF IOLと多焦点IOLの光学的性能差を数値データとともに詳細に検証します。
📚 1. メタアナリシスが示すEDOFの近方視力の限界
EDOFレンズと三焦点IOLの比較に関する最も包括的なエビデンスは、複数のメタアナリシスから得られている。
📖 Karamら(2023)——22研究・2,200眼のメタアナリシス
Karamら(2023)は22研究・2,200眼を対象とした更新版メタアナリシスにおいて、三焦点IOLがEDOFに対して以下の優位性を報告した[1]。
- 📊 UNVA(裸眼近方視力):MD = 0.12 logMAR(P < 0.00001)→ 三焦点が有意に優位
- 📊 DCNVA(矯正下近方視力):MD = 0.12 logMAR(P = 0.002)→ 三焦点が有意に優位
- 📊 UDVA(裸眼遠方視力):MD = 0.00(P = 0.84)→ 有意差なし
- 📊 UIVA(裸眼中間視力):MD = 0.01(P = 0.68)→ 有意差なし
- 👓 近方眼鏡使用率:EDOF群48% vs 三焦点群12%(OR = 0.26, P = 0.02)
- 🌙 ハロー・グレア:両群間に有意差なし
📖 Zhongら(2021)——13研究(898三焦点眼 vs 624 EDOF眼)
Zhongら(2021)のメタアナリシスでも、三焦点IOLのUNVA優位性(MD = −0.143, P < 0.001)とCNVA優位性(MD = −0.149, P < 0.001)が確認されている[2]。唯一EDOFが統計的に優れた指標はUIVA(MD = 0.055, P = 0.005)であったが、その差はわずか0.055 logMARであり臨床的意義は限定的である[2]。
📖 Tavassoliら(2024)——Cochrane系統的レビュー
2024年にTavassoliらが報告したCochrane系統的レビューは、5件のRCTのみを厳格に選定し(全てTECNIS Symfony ZXR00をEDOFとして使用)、三焦点IOLが近方視力と近方眼鏡非依存性において優れる可能性を示した[3]。ハロー・グレアなどの光学的愁訴には両群間で臨床的に意味のある差は検出されなかった[3]。
主要メタアナリシスの統合結果
| パラメータ | EDOF(Symfony/Vivity) | 三焦点(PanOptix/AT LISA tri/FineVision) | 統計的有意差 |
|---|---|---|---|
| UDVA(裸眼遠方視力) | 同等 | 同等 | NS(P = 0.84)[1] |
| UIVA(裸眼中間視力) | わずかに良好(+0.02〜0.06 logMAR) | 同等 | EDOF微差(一部P < 0.05)[2] |
| UNVA(裸眼近方視力) | 劣位(0.10〜0.16 logMAR劣る) | 優位 | P < 0.00001[1] |
| 近方眼鏡非依存率 | 33〜52% | 83〜100% | P < 0.0001[1][10] |
| ハロー/グレア | 同等 | 同等 | NS[1][3] |
| 患者満足度 | 高い | 高い | NS[4] |
この表から明らかなように、EDOFレンズの「光学的副作用が少ない」という臨床微メリットは、メタアナリシスレベルのエビデンスでは支持されていない。
📈 2. デフォーカスカーブが暴く焦点範囲の真実
デフォーカスカーブは、各IOLの「真の」焦点範囲を客観的に評価する最も重要な臨床指標である。
🔬 Monacoら(2017)のRCT
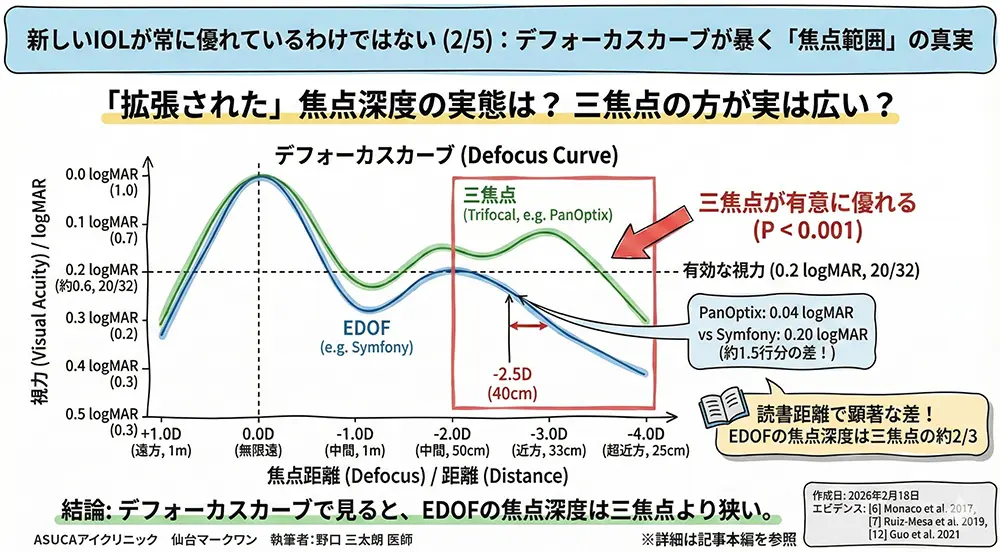
Monacoら(2017)のRCTでは、PanOptix三焦点IOLとTECNIS Symfony EDOFの両眼デフォーカスカーブを比較し、−2.0D〜−4.0Dの範囲でPanOptixが有意に優れる(P < 0.001)ことを示した[6]。具体的には、−2.5D(40cm近方)でのDCNVAはPanOptix 0.04 ± 0.06 logMAR vs Symfony 0.20 ± 0.07 logMAR(P < 0.001)であり、0.16 logMARの差は臨床的に約1.5行の視力差に相当する[6]。
🔬 Ruiz-Mesaら(2018)の前向き比較研究
Ruiz-Mesaら(2018)の前向き比較研究でも同様の結果が確認されている。40cmでのDCNVAはPanOptix 0.04 ± 0.06 vs Symfony 0.20 ± 0.07 logMAR(P < 0.001)であり、この差は被験者の読書体験に直接的な影響を及ぼす[7]。
デフォーカスレベル別の詳細解析(Guoら 2021)
| デフォーカス | EDOFの優位(−)/三焦点の優位(+) | 臨床的意味 |
|---|---|---|
| −0.5D〜−1.5D | EDOFがわずかに優位(MD: −0.03〜−0.06) | 中間距離でEDOF微差[12] |
| −2.0D〜−2.5D | 三焦点が有意に優位 | 近方視力で明確な差[6][7] |
| −2.5D〜−4.0D | 三焦点が有意に優位(P < 0.01) | 読書距離で顕著な差[6][12] |
VA ≥ 0.2 logMAR(20/32相当)を維持できるデフォーカス範囲は、三焦点IOLで0D〜−3.0D(無限遠〜33cm)であるのに対し、Symfonyは0D〜−2.0D(無限遠〜50cm)にとどまる[6][8]。つまり、EDOFレンズの「拡張された」焦点深度は、実際には三焦点IOLの焦点範囲の3分の2程度に過ぎない。この事実は、デフォーカスカーブを実際に測定しなければ把握できず、遠方・近方のSnellen視力のみでは検出不可能である。
🏥 FDA承認前データ解析(Moshirfarら 2023)
Moshirfarら(2023)のFDA承認前データ解析は、さらに衝撃的な数値を提示している。両眼裸眼で20/20以上を達成した割合は、近方においてSynergy 47%、PanOptix 50%に対してSymfony わずか22%(P < 0.0001)であった[9]。この結果は、EDOFの近方性能の限界を端的に示している。
⚛️ 3. IOL光学設計の物理学:回折・屈折・色収差の数理
IOLの光学性能を正確に評価するためには、その設計原理の物理学的理解が不可欠である。
🔵 フレネルゾーンプレートの原理
回折型多焦点IOLの設計はフレネルゾーンプレートの原理に基づいており、n番目の回折ゾーンの半径は以下の式で与えられる。
rn = √(2nλf)
λ:設計波長、f:回折成分の焦点距離。加入度数 Padd との関係は Padd = 2λ / r12 で表される。各ゾーンの面積はπr12で等しく、周辺部に向かってゾーン幅は漸減する。
🔵 回折効率とsinc²関数
回折効率は、ブレーズ角(鋸歯状プロファイル)の位相遅延パラメータαによって決定され、m次回折光の効率はスカラー回折理論により以下のsinc²関数で記述される[18]。
ηm = sinc²(α − m)
α = (λ0/λ) · [n(λ) − 1] / [n(λ0) − 1]
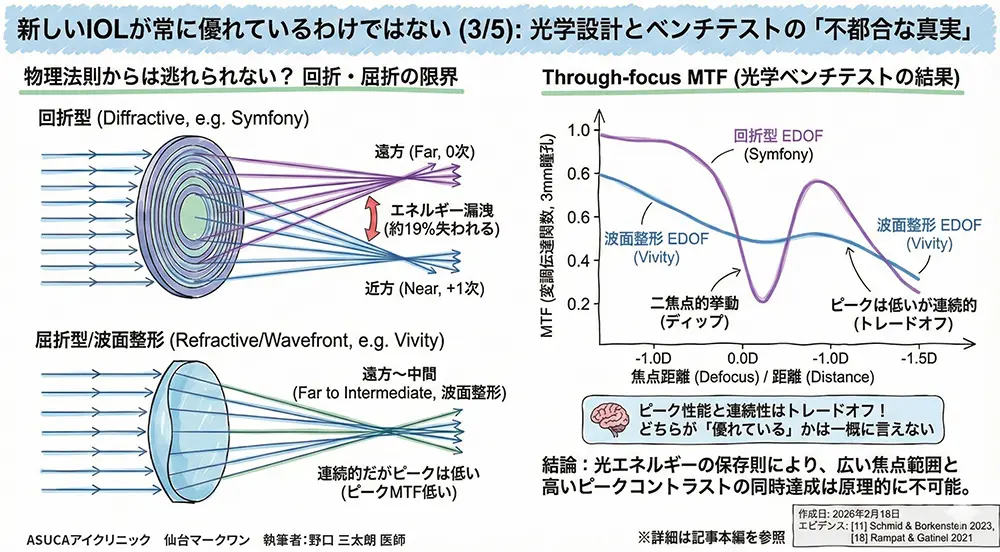
設計波長(α = 1)では1次回折光の効率は理論上100%だが、他の波長では光エネルギーが他の回折次数に漏洩する。二焦点IOLでは、遠方(0次)と近方(+1次)への光配分は位相遅延量 p = h(nlens − nmedium)/λ によって η0 = cos²(πp)、η1 = sin²(πp) として制御される。50/50分配(p = 0.5)では各焦点に約40.5%が配分され、約19%のエネルギーが不要な回折次数に失われる。
🔵 色収差補正の数理
色収差補正は、回折光学素子の特異な分散特性に依拠する。屈折素子のアッベ数 Vd = (nd − 1)/(nF − nC) が正値(IOL材料で37〜58)であるのに対し、回折素子のアッベ数は負値である[18]。
Vdiff = λd / (λF − λC) = 587.6 / (486.1 − 656.3) ≈ −3.45
この符号の反転により、回折素子は屈折素子と逆方向の色収差を生じ、両者を組み合わせることで色収差補正が可能となる。
色消し条件は以下で与えられる[18]。
Pref/Vref + Pdiff/Vdiff = 0
Pref:屈折成分の屈折力、Pdiff:回折成分の屈折力、Vref:屈折成分のアッベ数、Vdiff:回折成分のアッベ数
TECNIS Symfonyはこの原理を応用した色消し回折パターンを採用し、+1次回折光の負のLCA(縦色収差)で眼の正のLCA(偽水晶体眼で約1.0〜1.77D)を補正しつつ、焦点深度を拡張している[5][18]。しかし、この設計は本質的にlow-add二焦点であり、Through-focus MTF上では2つのピーク間に明確なディップが観察される[11]。
🔬 4. Through-focus MTFとStrehl比:光学ベンチが示す不都合な真実
光学ベンチ測定は、臨床測定では捉えきれないIOLの本質的な光学特性を明らかにする。
📐 MTFとStrehl比の定義
MTF(変調伝達関数)はOTF(光学伝達関数)の絶対値として定義される[11]。
MTF(ν) = |OTF(ν)|
ISO 11979-2に基づき、50 lp/mmおよび100 lp/mmでの3.0mmおよび4.5mmアパーチャにおけるMTFが標準的に測定される。
Strehl比は結像系の回折限界性能に対する実際の性能比を表し、以下のMaréchal近似で波面誤差から推定できる[11]。
S ≈ exp[−(2π σW/λ)²]
σWはRMS波面誤差。回折限界(S ≥ 0.8)はλ/14 RMS波面誤差に対応する。多焦点IOLでは光エネルギーが複数焦点に分配されるため、各焦点におけるStrehl比は本質的に単焦点IOLより低下する。
3種EDOF IOLのThrough-focus MTF比較(SchmidとBorkenstein 2023)
| IOL | 3mm主ピーク | 3mm副ピーク | 4.5mm主ピーク | 4.5mm副ピーク |
|---|---|---|---|---|
| TECNIS Symfony(回折型EDOF) | 0.420 | 0.372 | 0.468 | 0.318 |
| AcrySof IQ Vivity(波面整形EDOF) | 0.325 | 0.190 | 0.350 | 0.110 |
| LuxSmart Crystal(波面整形EDOF) | 0.250 | 0.335 | 0.245 | 0.250 |
💡 この結果が示す2つの重要事実
第一に、Symfonyは最も高いピークMTF値を持つが、明確な二焦点的挙動(2つのピーク間にディップ)を示し、「連続的な焦点深度拡張」という商業的説明とは乖離がある[11]。第二に、Vivityはピーク値が低いものの、より連続的なThrough-focus挙動を示す[11]。すなわち、ピーク性能と連続性はトレードオフであり、どちらが「優れている」かは一義的に決まらない。
📊 コントラスト感度に関するエビデンス
- 🔹 Kim SJら(2024):VivityがPanOptixに対して中高空間周波数(12, 18 cpd)のコントラスト感度で有意に優位(明所・暗所とも)[4]
- 🔹 Paikら(2020):Symfony EDOFのコントラスト感度が三焦点FineVisionおよびMix-and-Match群より低いという想定外の結果[22]
- 🔹 Guoら(2021)メタアナリシス:明所・暗所いずれのコントラスト感度においてもEDOF群と三焦点群に有意差なし[12]
これらの結果を総合すると、「EDOFはコントラスト感度が優れる」という一般的通念は、非回折型EDOF(Vivity)においてのみ一定のエビデンスがあり、回折型EDOF(Symfony)には必ずしも当てはまらない[4][12][22]。
🌟 5. ハロー・グレアにおけるEDOF優位の神話
EDOFレンズの最大のセールスポイントとされる「光学的副作用の少なさ」は、エビデンスに基づくと大幅に修正が必要である。
📊 客観的測定データ
Escandón-Garcíaら(2018)はLight Distortion Analyzer(LDA)を用いた客観的測定において、Symfony EDOFのLight Distortion Index(LDI)が34.6 ± 16.0%と、FineVision三焦点やPanOptix三焦点と同等ないしそれ以上であることを報告した(P = 0.237)[13]。さらに、QoV(Quality of Vision)の不快感スコアはSymfonyが有意に高い結果であった(47.2 ± 16.0 vs FineVision 32.8 ± 16.0、P = 0.011)[13]。著者らは「客観的に測定されたdysphotopsiaはEDOF IOLにおいて三焦点IOLと比較して減少していない」と明確に結論づけている[13]。
📊 ハローの質的分析
Teshigawaraら(2021)は、コンピュータベースのハローシミュレータを用いた定量的研究において、興味深い結果を報告した[14]。
- PanOptixのハローサイズ:Symfonyより有意に大きい(P < 0.05)
- Symfony의 ハロー強度(輝度):PanOptixより有意に高い(P < 0.05)
つまり、PanOptixは「小さく明るい」ハロー、Symfonyは「大きく暗い」ハローを生じ、質的に異なる光学的干渉パターンを呈するのであり、単純な優劣比較は不適切である[14]。
Mencucciら(2018)の3群比較(PanOptix、AT LISA tri、Symfony各40眼)では、全IOL群の70%の患者がハローを、50%がグレアを経験し、群間に有意差はなかった[15]。
🏥 非回折型EDOF(Vivity)の例外的優位性
非回折型のVivity EDOFのみが、dysphotopsiaプロファイルにおいて明確な優位性を示している。Hovanesianら(2022)では、Vivity患者の85%が「ない」または「わずか」のグレア・ハローと回答したのに対し、PanOptixは69%であった(P < 0.03)[10]。ただし、この優位性と引き換えに、完全な眼鏡非依存率はVivity 33% vs PanOptix 83%(P < 0.0001)という劇的な差が存在する[10]。
Karamら(2023)のメタアナリシス[1]、およびTavassoliら(2024)のCochrane系統的レビュー[3]は、いずれもEDOF群と三焦点群のハロー・グレアに有意差なしと結論づけている。「EDOFは光学的副作用が少ない」という主張は、プールされたエビデンスによって支持されていない。
⚠️ 6. 見落とされる評価指標:なぜ多くの眼科医がIOLの真の性能を把握できないのか
IOLの性能評価における最も深刻な問題は、評価手法の標準化の欠如と臨床で使用される指標の不十分さにある。
📏 デフォーカスカーブ標準化の問題
Wolffsohnら(2022)はJCRSにおいて、デフォーカスカーブの生成に影響する要因として瞳孔径、コントラストレベル、球面vs円柱デフォーカス、単眼vs両眼測定、検査チャートの種類、ジオプター範囲・ステップ幅を挙げ、研究間比較を可能にする標準化された方法論が存在しないことを指摘した[17]。
Buckhurstら(2012)も同様に、焦点深度測定に適切とみなされるVAの閾値(0.2 logMARか0.3 logMARか)についてコンセンサスが存在しないことを報告している[25]。Taña-Riveroら(2024)は、Landolt C視標とETDRS視標でデフォーカスカーブが約1行分異なることを示し、検査チャートの選択自体が結果を左右することを明らかにした[24]。
多焦点IOLの適切な評価に最低限必要な5要素
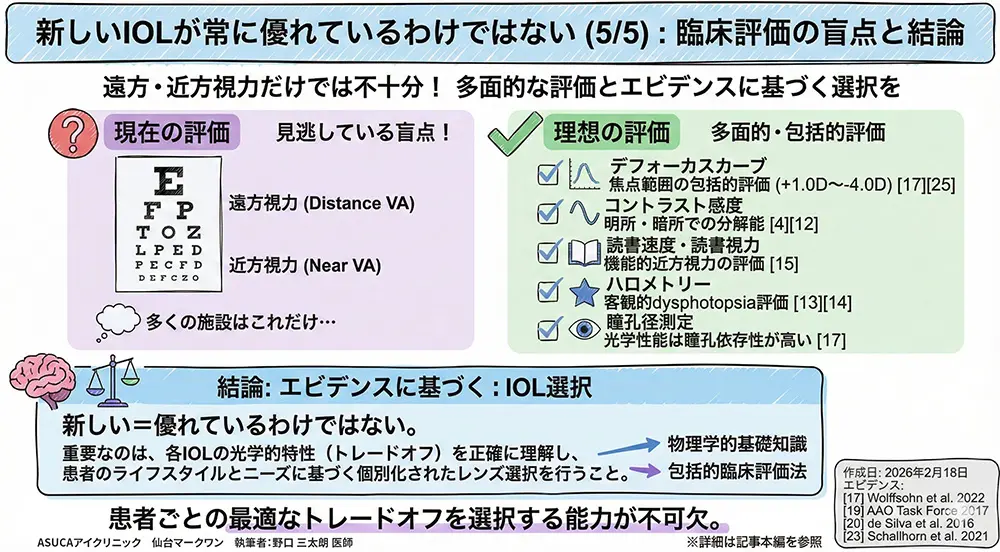
遠方視力のみでの評価がいかに不十分であるかは、de Silvaら(2016)のCochrane系統的レビューにおいて「IOLの有効性を要約する単一のアウトカム指標は存在しない」と明確に記されている[20]。多焦点IOLの適切な評価には、以下の5つの要素が最低限必要である。
| 評価項目 | 具体的手法 | 評価対象 |
|---|---|---|
| 📈 デフォーカスカーブ | +1.0D〜−4.0D、0.5Dステップ | 焦点範囲の包括的評価[17][25] |
| 👁️ 明所・暗所コントラスト感度 | CSV-1000またはPelli-Robson | 光学的分解能の評価[4][12] |
| 📖 読書速度・読書視力 | MNRead、Radnerチャート | 機能的近方視力の評価[15] |
| 🌙 ハロメトリー/光散乱解析 | Light Distortion Analyzer等 | 客観的dysphotopsia評価[13][14] |
| 🔵 瞳孔径測定 | 赤外線瞳孔計 | 多焦点IOLの光学性能は瞳孔依存性が高い[17] |
しかし現実には、多くの臨床施設では遠方視力と近方視力の2点測定のみでIOLの性能を判断している。AAO(米国眼科学会)のTask Force(MacRaeら、2017)はEDOF IOLの最低評価基準として、モノフォーカル対照と比較した0.50D以上の焦点深度拡張の証明を求めているが、この基準すら日常臨床で遵守されることは稀である[19]。
🏷️ 商業的命名の問題
RampatとGatinel(2021)はOphthalmology誌の総説で、2020年時点で市場に約100種のIOLが存在し、その商業的命名(「X-WAVE」「OptiBlue」等)が「情報的というより神秘的」であることを指摘した[18]。Journal of Ophthalmic and Vision Research(2024)の論説は、この混乱が「外科医が適切なレンズ選択を行うことを妨げている」と批判している[23]。
💰 業界スポンサーシップの影響
業界スポンサーシップの影響も無視できない。Lundhら(2017, 2020更新)のCochrane系統的レビュー(75論文対象)では、以下の結果が示されている[21]。
- 企業スポンサー研究は好意的な有効性結果を示す確率:RR = 1.27(95% CI: 1.17–1.37)
- 好意的な結論を導く確率:RR = 1.34(95% CI: 1.19–1.51)
- この傾向は薬剤・医療機器間で差がなかった(交互作用検定 P = 0.98)
IOL分野においても、新製品の発表と同時に発表される「sponsored study」の結果を無批判に受容することのリスクを認識すべきである。
🎯 7. 結論:エビデンスに基づくIOL選択と評価の転換
本稿で検討したエビデンスから、以下の結論が導かれる。
⚖️ EDOF IOLの位置づけ
EDOF IOLは三焦点IOLの「進化形」ではなく、異なるトレードオフプロファイルを持つ代替設計である。 近方視力と眼鏡非依存性では三焦点IOLが明確に優れ[1][2][3]、dysphotopsiaでは非回折型EDOF(Vivity)のみが優位性を示す[10]。回折型EDOF(Symfony)は光学的副作用においても三焦点IOLと同等のエビデンスしかない[1][3][13]。
🔬 光学ベンチデータの示唆
Through-focus MTFデータは、Symfonyが高いピーク値を持つものの本質的には低加入二焦点レンズであること、Vivityは連続的な焦点プロファイルを提供するがピーク光学性能では劣ること、そしてこのトレードオフが不可避の物理法則に由来することを示す[11]。光エネルギーの保存則により、広い焦点範囲と高いピークコントラストの同時達成は原理的に不可能であり、これはどんな新技術でも覆せない。
🏥 臨床評価の変革の必要性
臨床評価の観点からは、遠方・近方2点のVA測定のみに依存する現行の多くの施設の評価法は、IOLの光学的特性の大部分を見逃している[17][20][25]。デフォーカスカーブ、コントラスト感度(明所・暗所)、ハロメトリー、読書速度を含む包括的多面的評価の標準化と普及が急務である[19][23]。IOLの「世代」や「テクノロジー名」ではなく、標準化されたプロトコルに基づく客観的光学データによってレンズを評価し、患者のライフスタイルとニーズに基づく個別化されたレンズ選択を行うことが、真のevidence-based practiceである。
新しいレンズが常に優れているわけではない。 重要なのは、各IOLの光学的特性を正確に理解し、患者ごとに最適なトレードオフを選択する能力であり、そのためには物理学的基礎知識と包括的臨床評価法の両方が不可欠である。
📝 専門家向けまとめ
- ✅ メタアナリシス(22研究・2,200眼)でEDOF IOLの近方視力はlogMAR 0.12劣位、眼鏡非依存率は33〜52% vs 83〜100%
- ✅ Cochrane系統的レビューでハロー・グレアに有意差なし——「EDOF=dysphotopsia低減」は回折型では非支持
- ✅ Through-focus MTFでSymfonyの二焦点的挙動が確認——「連続적焦点拡張」との商業的説明は光学データと不一致
- ✅ 光エネルギー保存則により、焦点範囲拡大とピークコントラスト維持の同時達成は物理的に不可能
- ✅ 臨床評価はデフォーカスカーブ・CS・ハロメトリー・読書速度の多面的プロトコルへ転換すべき
📖 参考文献
📖 参考文献
[1] Karam M, Alkhowaiter N, Alkhabbaz A, et al. Extended Depth of Focus Versus Trifocal for Intraocular Lens Implantation: An Updated Systematic Review and Meta-Analysis. Am J Ophthalmol. 2023;251:52-70.
https://doi.org/10.1016/j.ajo.2023.01.024
[2] Zhong Y, Wang K, Yu X, et al. Comparison of trifocal or hybrid multifocal-extended depth of focus intraocular lenses: a systematic review and meta-analysis. Sci Rep. 2021;11:6699.
https://doi.org/10.1038/s41598-021-86222-1
[3] Tavassoli S, Ziaei H, Yadegarfar ME, et al. Trifocal versus extended depth of focus (EDOF) intraocular lenses after cataract extraction. Cochrane Database Syst Rev. 2024;7:CD014891.
https://doi.org/10.1002/14651858.CD014891.pub2
[4] Cho JY, Won YK, Park J, et al. Visual Outcomes and Optical Quality of Accommodative, Multifocal, Extended Depth-of-Focus, and Monofocal Intraocular Lenses in Presbyopia-Correcting Cataract Surgery. JAMA Ophthalmol. 2022;140(11):1045-1053.
https://doi.org/10.1001/jamaophthalmol.2022.3667
[5] Cochener B, Boutillier G, Lamard M, Auberger-Zagnoli C. A Comparative Evaluation of a New Generation of Diffractive Trifocal and Extended Depth of Focus Intraocular Lenses. J Refract Surg. 2018;34(8):507-514.
https://doi.org/10.3928/1081597X-20180530-02
[6] Monaco G, Gari M, Di Censo F, et al. Visual performance after bilateral implantation of 2 new presbyopia-correcting intraocular lenses: Trifocal versus extended range of vision. J Cataract Refract Surg. 2017;43(6):737-747.
https://doi.org/10.1016/j.jcrs.2017.03.037
[7] Ruiz-Mesa R, Abengozar-Vela A, Aramburu A, Ruiz-Santos M. Comparison of visual outcomes after bilateral implantation of extended range of vision and trifocal intraocular lenses. Eur J Ophthalmol. 2019;29(4):430-437.
https://pubmed.ncbi.nlm.nih.gov/28885672/
[8] Webers VSC, Bauer NJC, Saelens IEY, et al. Comparison of the intermediate distance of a trifocal IOL with an extended depth-of-focus IOL. J Cataract Refract Surg. 2020;46(2):193-203.
https://doi.org/10.1097/j.jcrs.0000000000000012
[9] Moshirfar M, Stoakes I, Theis J, et al. Assessing Visual Outcomes: A Comparative Study of US-FDA Premarket Approval Data for Multifocal and EDOF Lens Implants. J Clin Med. 2023;12(13):4365.
https://doi.org/10.3390/jcm12134365
[10] Hovanesian JA, Jones M, Allen Q. The Vivity Extended Range of Vision IOL vs the PanOptix Trifocal, ReStor 2.5 Active Focus and ReStor 3.0 Multifocal Lenses. Clin Ophthalmol. 2022;16:39-46.
https://doi.org/10.2147/OPTH.S345828
[11] Schmid R, Borkenstein AF. Enhanced Depth of Focus Intraocular Lenses: Through Focus Evaluation of Wavefront-Shaping versus Diffractive Optics. Biomed Hub. 2023;8(1):25-30.
https://doi.org/10.1159/000529234
[12] Guo Y, Wang Y, Hao R, et al. Comparison of Patient Outcomes following Implantation of Trifocal and Extended Depth of Focus Intraocular Lenses. J Ophthalmol. 2021;2021:1115076.
https://doi.org/10.1155/2021/1115076
[13] Escandón-García S, Ribeiro FJ, McAlinden C, et al. Through-focus vision performance and light disturbances of 3 new intraocular lenses for presbyopia correction. J Ophthalmol. 2018;2018:6165493.
https://pubmed.ncbi.nlm.nih.gov/29651343/
[14] Teshigawara T, Meguro A, Mizuki N. Halo size and intensity in pseudophakic eyes. Clin Ophthalmol. 2021;15:4141-4152.
https://doi.org/10.2147/OPTH.S327660
[15] Mencucci R, Favuzza E, Caporossi O, et al. Comparative analysis of visual outcomes, reading skills, contrast sensitivity, and patient satisfaction with two models of trifocal diffractive intraocular lenses and an extended range of vision intraocular lens. Graefes Arch Clin Exp Ophthalmol. 2018;256(10):1913-1922.
https://pubmed.ncbi.nlm.nih.gov/29980919/
[16] Schallhorn JM. Multifocal and Extended Depth of Focus Intraocular Lenses: A Comparison of Data from the United States FDA Premarket Approval Trials. J Refract Surg. 2021;37(2):98-104.
https://doi.org/10.3928/1081597X-20201111-02
[17] Wolffsohn JS, et al. Defocus curves: focusing on factors influencing assessment. J Cataract Refract Surg. 2022.
https://pubmed.ncbi.nlm.nih.gov/35137697/
[18] Rampat R, Gatinel D. Multifocal and extended depth-of-focus intraocular lenses in 2020. Ophthalmology. 2021;128:e164-e185.
https://pubmed.ncbi.nlm.nih.gov/33309899/
[19] MacRae S, Holladay JT, Glasser A, et al. AAO Task Force Consensus Statement for Extended Depth of Focus Intraocular Lenses. Ophthalmology. 2017;124(1):139-141.
https://pubmed.ncbi.nlm.nih.gov/27993458/
[20] de Silva SR, Evans JR, Kirthi V, et al. Multifocal versus monofocal intraocular lenses after cataract extraction. Cochrane Database Syst Rev. 2016;12:CD003169.
https://doi.org/10.1002/14651858.CD003169.pub4
[21] Lundh A, Lexchin J, Mintzes B, et al. Industry sponsorship and research outcome. Cochrane Database Syst Rev. 2017;2:MR000033.
https://pubmed.ncbi.nlm.nih.gov/28207928/
[22] Paik DW, et al. Comparison of visual outcomes in eyes implanted with mix-and-match, extended depth of focus, and trifocal intraocular lenses. Sci Rep. 2020;10:14832.
https://doi.org/10.1038/s41598-020-69318-y
[23] Schallhorn JM, et al. Multifocal and Accommodating Intraocular Lenses for the Treatment of Presbyopia: A Report by the AAO. Ophthalmology. 2021;128:1469-1482.
https://pubmed.ncbi.nlm.nih.gov/33581178/
[24] Fernández J, et al. Functional Classification of Intraocular Lenses Based on Defocus Curves. J Refract Surg. 2024.
https://pubmed.ncbi.nlm.nih.gov/38346117/
[25] Buckhurst PJ, Wolffsohn JS, et al. Multifocal Intraocular Lens Differentiation Using Defocus Curves. Invest Ophthalmol Vis Sci. 2012;53(7):3920-3926.
https://iovs.arvojournals.org/article.aspx?articleid=2188702
ASUCAアイクリニック 仙台マークワンは、白内障手術(眼内レンズ手術)、硝子体手術、ICL・IPCL、目の周りやまぶたなどを治療する手術専門クリニックです。
当院は、一人ひとりに精密な検査と時間を確保するため、完全予約制としております。
予約のページから予約の上お越しください。
ご不明な点がございましたら、LINEやお問い合わせページにて対応しております。
アクセス
宮城県仙台市青葉区中央一丁目2-3 仙台マークワン11F
仙台駅直結徒歩2分
*県外から当院で自費手術を受けられる方を対象とした「交通費負担軽減制度(手術代金より1万円の充当)」を設けております。詳細はスタッフにお問い合わせください。
免責事項本記事は教育・情報提供を目的としており、個別の医療相談や診断・治療の代替となるものではありません。眼科治療を検討される場合は、必ず眼科専門医にご相談ください。医学情報は日々更新されるため、最新情報の確認も重要です。